This is a demo store. No orders will be fulfilled.
D-荧光素体外实验方案
引言
荧光素是一种广泛用于体外成像的生物发光报告分子,可用于检测荧光素酶的表达。该水溶性底物适用于萤火虫荧光素酶(通常来源于 Photinus pyralis),在 ATP 和 Mg²⁺ 作为辅因子的存在下,并在有氧条件下,会发射特征性的黄绿色光。由于该反应依赖ATP,因此也可作为细胞存活与死亡的指示剂,通过检测代谢活性来反映生命状态。
萤火虫荧光素酶是研究基因表达中最灵敏且最易用的报告基因之一,常用于监测细菌、培养细胞以及转基因植物或动物中的启动子活性。该酶为约 61 kDa 的单体结构,不需要翻译后修饰即可具有活性。荧光素酶通过催化荧光素的氧化脱羧反应,产生具有已知最高反应效率之一的生物发光信号。在优化反应条件时,发射光的强度可与转录活性直接相关,因此该体系非常适合利用启动子/增强子元件来表征基因调控机制。
本手册提供了一种简便、经济且可靠的体外检测荧光素酶活性的实验方案。
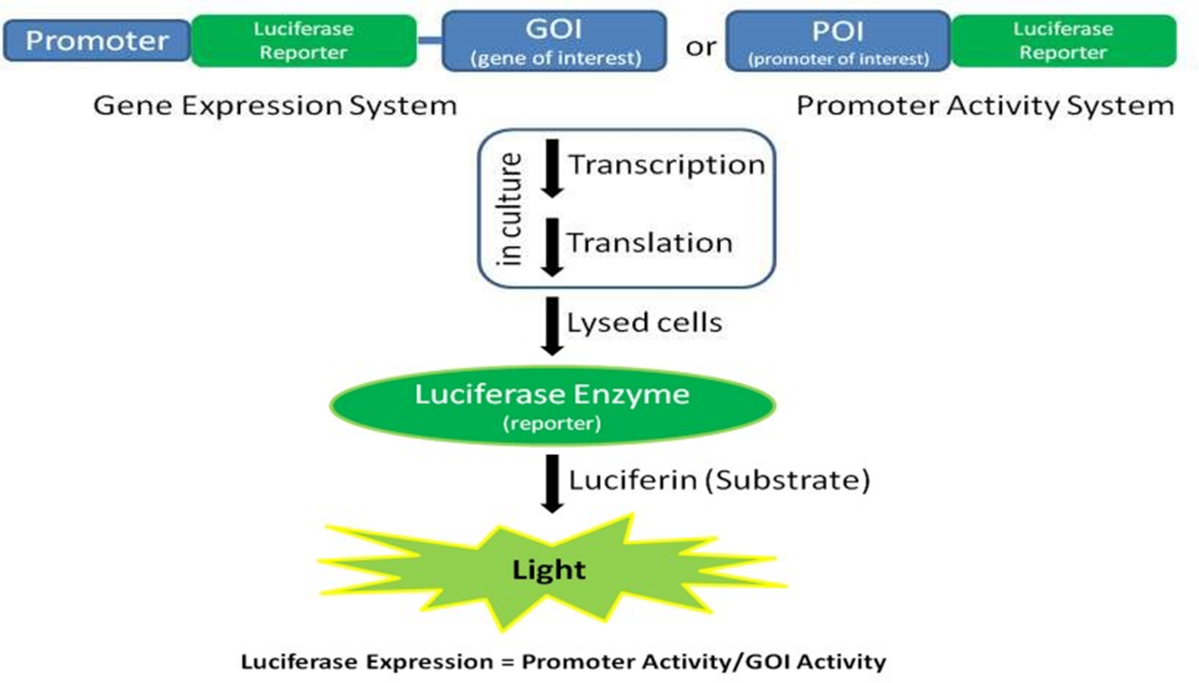
生物发光反应
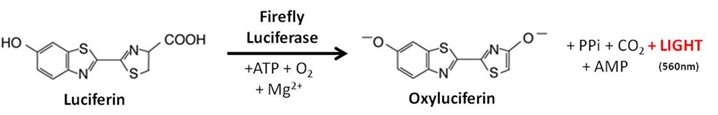
生物发光反应的灵敏度会受到温度、pH 值及底物浓度的影响。为获得最佳结果,我们建议遵循以下条件:
- 使用 pH 7.8 的缓冲液;
- 在使用前将所有试剂预温至室温;
- 在反应缓冲液中加入过量的 ATP 和 Mg²⁺。
当在含有荧光素酶的样品中加入荧光素时,光发射会在 0.3–0.5 秒内达到峰值,并迅速衰减,其半衰期约为 0.5–1 分钟。若在缓冲液中预先加入辅酶 A(CoA),可将该半衰期延长至 2–5 分钟。即使在反应开始后再添加 CoA,也仍能促进二次发光现象(Fraga,2008)。

推荐的荧光素酶检测缓冲液配方(改编自 Oba 等,2003):
- 100 mM Tris-HCl(pH 7.8)
- 5 mM MgCl₂ – 250 μM 辅酶 A(CoA)
- 150 μM ATP(Fraga,2008)
- 150 μg/mL D-荧光素(Aladdin)
可根据检测需求选择性添加 DTT 或 EDTA(Steghens,1998)。建议先进行预实验,以优化适用于特定细胞系的动力学曲线。
产品信息
- D-荧光素,钾盐
Aladdin 目录号:D1375449、D1375455、L120798
分子式:C11H7KN2O3S2
分子量:318.42 g/mol
- D-荧光素,钠盐
Aladdin 目录号:D1375459、D1375464、D115509
分子式:C11H7N2NaO3S2
分子量:320.32 g/mol
储存与操作:-20°C 保存,避光保护。
材料
- D-荧光素(钾盐/钠盐)
- 荧光素酶检测缓冲液(TMCA)
- Tris-HCl(pH 7.8)
- 氯化镁(MgCl₂)
- 辅酶 A(CoA,水合物)
- ATP(二钠盐水合物)
- 荧光素储备液(LSS)
- 磷酸盐缓冲液 PBS(不含 Ca²⁺ 和 Mg²⁺)
- 细胞裂解缓冲液(哺乳动物、细菌、酵母专用)
- 荧光素酶(用于校准/对照)
荧光素储备液 (LSS) 制备方法
1. 制备
将LSS配制为15mg/mL(100×)浓度,使用分子生物学级纯水(H₂O)溶解。
- 可立即使用,或分装后于-80°C保存,最长可保存1个月。
2. 在荧光素酶发光检测中的终浓度
- 荧光素底物LSS的最终浓度为150μg/mL(荧光素钾盐为471μM,荧光素钠盐为468μM)。
荧光素酶检测缓冲液(TMCA)制备方法
在分子生物学级纯水(H₂O)中分别制备各组分溶液,然后按比例混合成TMCA。浓度需根据最终使用需求进行调整:
1.制备500mMMgCl₂(100×)溶液
- a.称取476.05mgMgCl₂(摩尔质量95.21g/mol),溶于10mLH₂O。
- b.溶液可在室温保存。
2.制备25mMCoA(100×)溶液
- a.称取191.88mgCoA(摩尔质量767.53g/mol),溶于10mLH₂O。
- b.用5–10mLH₂O预润湿0.2µm过滤器。
- c.通过预润湿的过滤器进行无菌过滤,所得100×CoA溶液于-20°C保存。
3.制备15mMATP(100×)溶液
- a.称取82.67mgATP(摩尔质量551.14g/mol),溶于10mLH₂O。
- b.于-20°C保存。
4.制备400mMTris-HCl,pH7.8(4×)缓冲液
- a.称取4.85gTris碱(摩尔质量121.14g/mol),溶于85mLH₂O。
- b.用1MHCl调节pH至7.8,再用H₂O定容至100mL。
5.制备新鲜2×TMCA工作液(室温)
a.根据实验所需计算TMCA总量,将各组分按比例混合至2×工作浓度(H₂O配制),在荧光素酶检测中将稀释至1×。
示例(制备1mL的2×TMCA):
- 500µLTris-HCl(4×)
- 20µLMgCl₂(100×)
- 20µLCoA(100×)
- 20µLATP(100×)
- 用H₂O补足至1mL
可选:此阶段可加入DTT或EDTA。
细胞裂解缓冲液
可根据实验需求选择:
- 细菌细胞裂解缓冲液
- 哺乳动物细胞裂解缓冲液
- 组织培养裂解缓冲液
- 酵母裂解缓冲液
用于荧光素酶提取的细胞裂解物制备
贴壁(单层)培养vs.悬浮培养
细胞培养可大致分为两种体系:在基质上形成单层的贴壁培养(adherent)和悬浮培养(nonadherent)。大多数动物来源的细胞为依赖基质附着的细胞(血液系统或类似细胞系除外),需要适宜的基质以实现正常黏附,这类基质通常称为“经组织培养处理(tissue-culture treated)”的表面。然而,许多此类细胞系也可适应于悬浮培养。
悬浮培养不需要经组织培养处理的培养容器,但培养基应持续轻微搅动,以确保充分的气体交换并防止细胞死亡。此类培养应每日通过细胞计数监测其生长与密度,并可通过稀释的方式促进进一步增殖。
贴壁培养需每日在倒置显微镜下观察,以评估细胞融合度(confluence)。当细胞融合度达到80–90%时,应进行传代培养,以避免营养耗尽及随后的细胞死亡。贴壁细胞需要经组织培养处理的培养皿以获得最佳的附着与生长效果。虽然玻璃器皿可替代一次性塑料器皿,但必须彻底去除所有残留清洁剂,并在使用前进行适当的灭菌处理。
不同细胞系的黏附特性存在差异。多数情况下,使用胰蛋白酶(trypsin)或其他蛋白酶来使细胞脱离基质。但对于某些细胞系,尤其是在蛋白酶可能损伤细胞或影响膜表面标记/受体的情况下,可选择在少量培养基中使用细胞刮刀进行机械性脱附。
贴壁细胞培养的脱附步骤
(改编自Methods in Molecular Biology,第290卷:Basic Cell Culture Protocols)
1. 移除培养基
当细胞达到所需融合度时,吸去培养基。用2–3ml室温(RT)无钙、无镁的PBS轻轻冲洗细胞单层,以去除残留培养基。
2. 加入消化液
吸去PBS,加入3–4ml室温的胰蛋白酶–EDTA(T/E)溶液。于37°C孵育3–5分钟,并在倒置相差显微镜下观察细胞的脱附情况。
3. 终止消化并收集细胞
当细胞开始脱附时,将其转移至含有6–7ml含血清培养基(用于抑制胰蛋白酶)的离心管中。为回收所有细胞,可用5ml细胞/培养基混合液冲洗培养皿1–2次,并将冲洗液合并至离心管中。
4. 细胞计数并进入裂解步骤
使用血球计数板(hemacytometer)进行细胞计数,然后进入裂解步骤。
注意:在裂解前需对细胞进行离心和洗涤(见下文)。
真核细胞裂解(哺乳动物或酵母)
使用前准备
根据具体应用需求,可在裂解缓冲液中加入DTT和EDTA,使其最终浓度达到5mM。若实验需要二价金属离子,则应省略EDTA,并改为加入适当的二价金属盐。
蛋白酶抑制
如需抑制蛋白酶活性,应在提取过程中加入蛋白酶抑制剂混合物,以防止蛋白酶活性干扰实验结果。可选用以下产品:
- 蛋白酶抑制剂混合物(适用于哺乳动物细胞与组织提取,EDTA Free,100X),货号Aladdin P775091
- 蛋白酶抑制剂混合物(适用于真菌及酵母,EDTA Free,100X),货号Aladdin P775089
哺乳动物(Mammalian)
1. 收集细胞:以200–500×g离心5分钟收集细胞,轻轻弃去上清液。对于贴壁细胞,需先进行消化或刮取(参考上文相关部分),然后离心收集并去除上清液。
2. PBS冲洗:用5–10ml不含Ca²⁺和Mg²⁺的PBS冲洗细胞沉淀,弃去上清液后,轻轻敲击离心管使沉淀松散。用移液器在5–10mlPBS中轻柔地吹打重悬细胞,再次离心收集细胞。
3. 去除PBS:彻底弃去PBS洗液并丢弃。
4. 裂解准备:用移液器将剩余少量PBS中的沉淀轻轻吹匀。向细胞沉淀中加入哺乳动物细胞裂解缓冲液(Mammalian Cell Lysis Buffer)。每10ml高密度悬浮培养物,约加入1ml裂解缓冲液。
替代方法:每0.05g湿细胞沉淀加入1ml裂解缓冲液。如需获得更高浓度的裂解液,可适当减少缓冲液体积,此时可进行一次冻融循环以促进完全裂解。
5. 裂解反应:用移液器充分混匀细胞至均一悬液,将混合物置于冰上孵育15–30分钟,期间偶尔轻轻倒置离心管以促进裂解。
注意:冻融步骤并非必须,但进行1–2次循环通常有助于裂解且不会损害裂解液质量。
6. 离心收集裂解液:将裂解液在20,000×g下,于冷冻离心机中离心30分钟,收集澄清的上清液用于后续实验。
注意:沉淀中可能仍含有核蛋白及膜结合蛋白,如有需要,可使用专用去污剂进行提取。
酵母(Yeast)
1. 收集细胞:当培养物OD600达1.5–2.0时,以5,000×g离心5–10分钟收集酵母细胞。将沉淀重悬于等体积酵母悬浮缓冲液(Yeast Suspension Buffer)中,并按每100µl悬液加入1µlβ-巯基乙醇。
2. 均匀悬液:轻轻用移液器吹打混匀,4°C孵育5分钟,再次吹打使细胞均匀悬浮。
3. 加入Zymolyase®:轻轻弹击Zymolyase®小瓶混匀后,按每100µl酵母悬液加入10µl Zymolyase®。轻柔混合使其分布均匀。
4. 孵育与监测裂解:37°C孵育30–60分钟。可取25µl反应液与1ml酵母裂解缓冲液混合,并测定800nm吸光度以监测裂解进程。
5. 分离球形体:孵育后,以1,500×g离心5分钟,小心弃去上清液,保留球形体沉淀。
可选步骤:用5–10倍体积酵母悬浮缓冲液清洗沉淀,轻轻敲击管壁重悬,再按上述条件离心,弃去上清液。
6. 裂解球形体:将球形体沉淀重悬于2–3倍体积酵母裂解缓冲液(Yeast Lysis Buffer)中,轻轻吹打数次混匀,期间可不时倒置混匀,置冰上孵育30分钟。
注意:短暂的37°C孵育(1–3分钟)或轻度超声处理可进一步促进裂解;如需剪切基因组DNA,则必须进行超声。缓冲液与沉淀比例越高,裂解效率越好。
7. 收集裂解液:以20,000×g、4°C条件离心30分钟,小心收集澄清的上清液,可直接用于分析。
注意:额外的酵母裂解缓冲液可单独购买,并可用于后续的层析、透析等实验。
商标声明:Zymolyase®是KirinBreweryCo.Ltd.注册的商标
细菌细胞
使用前准备
- 缓冲液配置:根据具体应用需求,可在细菌细胞裂解缓冲液(Bacterial Cell Lysis Buffer)中加入DTT和EDTA,使其最终浓度均为5mM。
- 若应用需要二价金属离子,则省略EDTA,改为加入适宜的二价金属盐,使最终浓度达到5mM。
- 抑制蛋白酶活性:若需防止蛋白酶降解,在提取过程中应加入蛋白酶抑制剂混合液,以保护蛋白质(参考适用于细菌细胞裂解液的无EDTA蛋白酶抑制剂混合液,100×,Aladdin P776695)。
蛋白提取与核算同步去除
1. 收集细胞:当培养物OD600介于1.5–3.0之间时,以5,000×g离心10分钟收集细菌细胞沉淀。将沉淀重悬于其体积5–10倍的细菌裂解缓冲液中(例如,25µL沉淀使用125–250µL缓冲液)。
2. 初步悬浮:轻轻用移液器吹打样品直至均匀。将悬液置于冰上或4°C孵育5分钟,再次轻柔吹打以确保完全混匀。
3. 加入溶菌酶:解冻溶菌酶溶液并涡旋混匀。按每100µL细胞悬液加入5µL溶菌酶(已溶于细菌裂解缓冲液中),然后轻轻混合。
4. 孵育:37°C孵育30–60分钟。
可选:取25µL悬液,稀释于1mL细菌裂解缓冲液中,在590nm测定吸光度以监测裂解进程。
5. 完成裂解:孵育结束后,轻轻倒置离心管数次以完成裂解。如有需要,可使用窄口枪头吹打,或通过20号针头反复推拉以进一步破碎细胞。
注意:额外的细菌裂解缓冲液可单独购买,用于后续的层析或透析等实验。
6. 去除核酸:在裂解过程中,DNA与RNA会被部分降解,从而降低裂解液黏度;残留的部分DNA片段通常不会影响后续步骤。若需彻底去除核酸,可在配置细菌裂解缓冲液时省略EDTA,并在裂解结束后补加EDTA至最终浓度2.5mM。
7. 澄清裂解液:以20,000×g、4°C条件离心30分钟,收集澄清的上清液用于分析。
球形体形成法蛋白提取
适用于需避免溶菌酶污染的情况。
1–4步骤同上方法的细菌蛋白提取流程,然后继续:
5. 分离球形体:孵育结束后,以200–500×g离心10分钟,轻轻弃去上清液,保留球形体沉淀。
- 可选:将球形体沉淀重悬于5–10倍体积的细菌悬浮缓冲液(Bacterial Suspension Buffer)中,重复上述离心步骤,弃去上清液。
6. 裂解球形体:将球形体沉淀重悬于适量细菌裂解缓冲液中(约为沉淀体积的2–3倍),用移液器轻柔吹打数次混匀,期间可偶尔倒置。样品置冰上孵育30分钟。为进一步提高裂解效率,可在37°C孵育1–3分钟或进行短暂超声处理。
注意:缓冲液与沉淀体积比例越高,裂解效率通常越好。
7. 收集裂解液:以20,000×g、4°C条件离心30分钟,收集澄清的上清液(裂解液),可直接用于后续分析。
包涵体分离:
在完成裂解步骤后,以30,000×g、4°C条件离心30分钟,收集包涵体沉淀。将沉淀用10倍稀释的细菌裂解缓冲液清洗两次(例如,将沉淀重悬于稀释缓冲液中,再次离心收集包涵体)。纯化后的包涵体可用于溶解及蛋白质复性实验。
荧光素酶校准曲线
为了在样品中准确定量萤光素酶水平,必须先确定所用发光检测仪(luminometer)的线性检测范围。这样可以确保光强读数的可靠性,并避免在高发光水平下出现信号饱和。
1. 制备稀释系列:将萤光素酶(可来自细胞培养裂解液或纯化的萤光素酶)稀释于1×裂解缓冲液中(纯化萤光素酶可用PBS)并补充1mg/ml BSA(BSA有助于稳定稀释后的萤光素酶)。
- 设置一个无萤光素酶的对照样品,用于测定背景发光值。
- 纯化萤光素酶储液配方:将1mg萤光素酶溶解于100mMTris-HCl(pH7.8)和5mMMgCl₂中。
a.储液可分装后于–20°C保存,或与等体积100%甘油混合后于–20°C保存(此时储液在该温度下保持不冻结)。
b.冷冻储液或含甘油储液在此储存条件下至少可保持活性两年。
2. 准备反应体系:向比色皿或96孔板的孔中加入100µl2×TMCA(最终浓度为1×)。
3. 加入LSS:向每个样品中加入2µl100×LSS(最终浓度为1×)。
4. 加入萤光素酶稀释液:向比色皿或孔中加入98µl稀释后的萤光素酶储液或裂解液。室温避光孵育5–10分钟(此步骤可稳定发光信号,确保校准曲线测量的准确性)。
- 为保证一致性,所有样品应孵育完全相同的时间后再读数。
- 注意:上述体积是基于加入100×LSS以获得最终1×TMCA浓度计算的。如需不同总反应体积,请按比例调整配方。
5. 测量发光值:使用发光检测仪读取光输出信号。
6. 绘制校准曲线:生成萤光素酶校准曲线,并确定光输出与细胞数(或与萤光素酶µg数量)的关系。
提示:如果检测结果未能得到合适的线性关系,可适当降低萤光素浓度。
荧光素酶发光检测实验
萤光素酶发光检测的效果会受到所使用发光检测仪类型的影响——无论是手动型、带进样器的单管型,还是板式读取型发光检测仪。
请务必参考所用仪器的用户手册,了解其进样功能及程序设定方法。
注意:LSS的浓度可能需要根据您的发光检测仪的进样体积要求进行调整。
在反应混合液中,TMCA的最终浓度应为1×。应调整裂解液与LSS的用量,使总反应体积与预定的最终TMCA体积一致。
示例1–手动型发光检测仪(最终反应体积:200µl)
1. 向干净的发光检测比色皿中加入100µlTMCA。
2. 向比色皿中加入50–98µl裂解液。
3. 如有需要,用H₂O补足总体积至198µl。
4. 加入2µlLSS(最终浓度1×),立即在发光检测仪上读取信号。
示例2–带进样功能的发光检测仪
(单个样品或微孔板;最终反应体积:200µl)
1. 向发光检测比色皿或96孔板(建议使用纯白色平底板)的每个孔中加入100µlTMCA。
2. 向比色皿或孔中加入50–98µl裂解液。
3. 如有需要,用H₂O补足总体积至198µl。
4. 在仪器上设置程序,使其自动注入LSS,设定2–5秒延迟,并记录发光信号10秒。
参考文献
Bai,X.,等.(2010).体外培养和新鲜分离的脂肪组织来源干细胞均可在急性心肌梗死后改善心脏功能.《欧洲心脏杂志》(EuropeanHeartJournal),31(4),489–501.
Fraga,H.(2008).萤火虫发光:历史回顾与最新进展.《光化学与光生物科学》(Photochemical&PhotobiologicalSciences),7(2),146–158.
Helgason,C.D.,&Miller,C.L.(2005).《分子生物学方法,第290卷:基础细胞培养技术(第三版)》(MethodsinMolecularBiology,vol.290:BasicCellCultureProtocols,ThirdEdition).HumanaPress.
Oba,Y.,Ojika,M.,&Inouye,S.(2003).萤火虫荧光素酶是一种双功能酶:ATP依赖的单加氧酶和长链脂酰辅酶A合成酶.《欧洲分子生物化学学会快报》(FEBSLetters),540(1),251–254.
Seliger,H.H.,&McElroy,W.D.(1960).萤火虫生物发光的光谱发射与量子产率.《生物化学与生物物理档案》(ArchivesofBiochemistryandBiophysics),88(1),136–141.
Steghens,J.P.,Min,K.L.,&Bernengo,J.C.(1998).萤火虫荧光素酶具有两个核苷酸结合位点:核苷酸单磷酸与辅酶A对发光光谱的影响.《生物化学杂志》(BiochemicalJournal),336(Pt1),109.
 首页
首页 400-620-6333
400-620-6333
