This is a demo store. No orders will be fulfilled.
1-氢硅氮烷

简介
1-氢硅氮烷,如图1所示,是一种用途广泛的氢化物试剂。它可用于各种还原反应,从醛和酮合成醇、胺、其手性衍生物和酯。1-6与其他硅烷相比,它的相对反应性,加上其水分稳定性和易处理性,使其成为一种有吸引力的还原剂选择。

图1. 1-氢硅氮烷
Frye等人于1961年报道了1-氢硅氮烷作为稳定的五配位烷氧基硅烷的开创性例子。7 1-氢硅氮烷的一个关键特征在于其笼状结构,这促进了氮和硅之间形成配位键。7-9 超配位有机硅烷在硅中心表现出增强的电敏感性,导致配体处的电子密度增加。10 尽管1-氢硅氮烷具有许多有益的性质,但它们在有机合成中作为试剂尚未得到广泛的应用。11
1976年,Eaborn和他的团队是探索1-氢硅氮烷作为氢化物来源的先驱,为其在还原六个不同官能团方面的应用提供了一个未经优化的例子。12由于Si-H键向氢的极化,氢硅烷起着氢化物来源的作用。13 1-氢硅氮烷中氮和硅之间的分子内配位增强了Si-H键的反应性,使其成为一种有效的氢化物供体。8,9尽管其刚性结构使其具有高稳定性,但最初的工作只提供了对1-氢硅氮烷作为还原剂潜力的初步见解。直到最近,从2016年开始,阿德勒小组才报道了利用1-氢硅氮烷的有效合成方法。1-6

图2. 利用1-氢硅氮烷作为氢化物还原剂的方法
1-氢硅杂环丁烷应用的优势
1-氢硅氮烷在空气和水分存在下是一种稳定的还原剂,适用于露天台式反应。它无毒、用户友好,并随着时间的推移保持其完整性。2 作为金属氢化物还原的更安全替代品,它提供了在温和条件下操作的简单方法。这种还原剂与许多官能团相容,表现出化学选择性,并产生无毒副产物。此外,它具有可扩展性,可以在没有金属的情况下使用,并且能够合成具有生物学意义的分子和药物。
代表性应用
1. 直接还原性胺化
直接还原胺化(DRA)是合成仲胺和叔胺最常用的技术。14 有效的DRA方法需要化学选择性氢化物源来还原亚胺或亚胺中间体,而不影响初始羰基或其他官能团。1-氢硅氮烷是一种高反应性的还原剂,由于其与各种官能团的相容性,非常适合用于DRA。1,2 研究表明,1-氢硅氮烷在DRA与醛/酮和仲胺的反应中具有广泛的适用性,可以生产叔胺(图3),展示了其对可还原基团和常见保护基团的优异耐受性。此外,在乙酸中使用醛/酮与1-氢硅氮烷合成仲胺(图3)。值得注意的是,即使在同一分子上存在酮取代基的情况下,DRA与1-氢硅氮烷的反应对醛也表现出化学选择性。因此,氨基醇可以使用1-氢硅氮烷在一锅法还原过程中合成(图4)。3

图3. 使用1-氢硅氮烷的直接还原胺化。[a]无水乙醇,相对温度[b]无水乙醇,70˚C

图4. 使用1-氢硅氮烷对酮醛进行两步一锅串联DRA/还原
许多关键胺表现出手性,使不对称非对映选择性还原胺化(DRA)成为一个关键过程。为了实现对映选择性,可以在前手性酮与芳胺的DRA中使用大型手性磷酸催化剂,利用1-氢硅氮烷作为还原剂。这使得手性胺的生产具有高转化率和优异的对映体过量(见图5)。6


图5. 使用1-氢硅氮烷和手性磷酸催化剂的不对称DRA
2. 酮的还原
当加入路易斯碱tBuOK时,1-氢硅氮烷被激活,能够在温和的条件下将各种酮还原为相应的醇,而不会产生挥发性或危险的硅烷(图6)。用1-氢硅氮烷还原酮可以实现高非对映选择性。此外,当包含手性添加剂时,酮的不对称还原可以表现出对映选择性,从而可以合成具有高对映体过量的手性醇(图7)。2,4

图6. 用1-氢硅氮烷还原酮

图7. 用1-氢硅氮烷和手性路易斯碱不对称还原前手性酮
3. 醛的还原
1-氢硅氮烷可用于将醛转化为相应的伯醇。当被NaOH激活时,它有效地将各种芳醛还原为苄醇,而不会产生醚或脱氧副产物(如图8所示)。1 与可还原的腈、硝基或苄基/烯丙基醚没有交叉反应。此外,杂芳基、多环芳基和脂肪醛也已使用1-氢硅氮烷有效还原。1

图8. 取代苯甲醛的还原
醛可以直接进行还原乙酰化反应生成酰化醇,这有利于合成酯或在合成过程中保护醇。该工艺可以提高多步合成路线的效率。通过在乙酸和醛的存在下使用1-氢硅氮烷作为还原剂,可以以良好到优异的收率合成各种乙酰酯(如图9所示)。值得注意的是,这种方法不会产生乙醚副产物。它证明了对醛的化学选择性,因为在探索底物范围时,同一分子上的酮仍然没有被还原。5
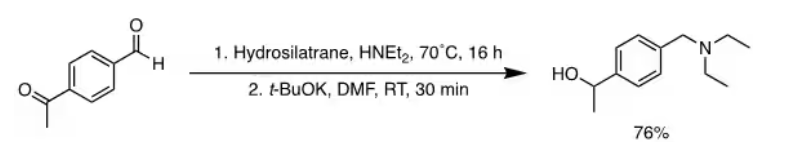
图9. 醛的直接还原乙酰化
参考文献
1. Skrypai V, Hurley JJM, Adler MJ. 2016. Silatrane as a Practical and Selective Reagent for the Reduction of Aryl Aldehydes to Benzylic Alcohols. Eur. J. Org. Chem.. 2016(12):2207-2211. https://doi.org/10.1002/ejoc.201501599
2. Varjosaari SE, Skrypai V, Suating P, Hurley JJM, Gilbert TM, Adler MJ. 2017. 1-Hydrosilatrane: A Locomotive for Efficient Ketone Reductions. Eur. J. Org. Chem.. 2017(2):229-232. https://doi.org/10.1002/ejoc.201601256
3. Varjosaari SE, Skrypai V, Suating P, Hurley JJM, Lio AMD, Gilbert TM, Adler MJ. 2017. Simple Metal-Free Direct Reductive Amination Using Hydrosilatrane to Form Secondary and Tertiary Amines. Adv. Synth. Catal.. 359(11):1872-1878. https://doi.org/10.1002/adsc.201700079
4. Varjosaari SE, Skrypai V, Herlugson SM, Gilbert TM, Adler MJ. 2018. Enantioselective metal-free reduction of ketones by a user-friendly silane with a reusable chiral additive. Tetrahedron Letters. 59(29):2839-2843. https://doi.org/10.1016/j.tetlet.2018.06.032
5.James, R.; Herlugson, S.; Varjosaari, S.; Skrypai, V.; Shakeel, Z.; Gilbert, T.; Adler, M. J. SynOpen 2019, 3, 1-3.
6.Skrypai V, Varjosaari SE, Azam F, Gilbert TM, Adler MJ. 2019. Chiral Brønsted Acid-Catalyzed Metal-Free Asymmetric Direct Reductive Amination Using 1-Hydrosilatrane. J. Org. Chem.. 84(9):5021-5026. https://doi.org/10.1021/acs.joc.8b03073
7.Frve CL, Vogel GE, Hall JA. 1961. TRIPTYCH-SILOXAZOLIDINES: PENTACOORDINATE BRIDGEHEAD SILANES RESULTING FROM TRANSANNULAR INTERACTION OF NITROGEN AND SILICON. J. Am. Chem. Soc.. 83(4):996-997. https://doi.org/10.1021/ja01465a058
8.Pestunovich V, Kirpichenko S, Voronkov M. Silatranes and Their Tricyclic Analogs.1447-1537. https://doi.org/10.1002/0470857250.ch24
9.Frye CL, Vincent GA, Finzel WA. 1971. Pentacoordinate silicon compounds. V. Novel silatrane chemistry. J. Am. Chem. Soc.. 93(25):6805-6811. https://doi.org/10.1021/ja00754a017
10.Oestreich M, Rendler S. 2005. Hypervalent Silicon as a Reactive Site in Selective Bond-Forming Processes. Synthesis. 2005(11):1727-1747. https://doi.org/10.1055/s-2005-869949
11.Puri JK, Singh R, Chahal VK. Silatranes: a review on their synthesis, structure, reactivity and applications. Chem. Soc. Rev.. 40(3):1791-1840. https://doi.org/10.1039/b925899j
12.Attar-bashi, M. T.; Eaborn, C.; Vencl, J.; Walton, D. R. M. J. Organomet. Chem. 1976, 117, 87-89.
13.Doyle MP, DeBruyn DJ, Donnelly SJ, Kooistra DA, Odubela AA, West CT, Zonnebelt SM. 1974. Silane reductions in acidic media. III. Reductions of aldehydes and ketones to alcohols and alcohol derivatives. General syntheses of alcohols, symmetrical ethers, carboxylate esters and acetamides. J. Org. Chem.. 39(18):2740-2747. https://doi.org/10.1021/jo00932a015
14.Podyacheva E, Afanasyev OI, Tsygankov AA, Makarova M, Chusov D. 2019. Hitchhikers Guide to Reductive Amination. Synthesis. 51(13):2667-2677. https://doi.org/10.1055/s-0037-1611788
 首页
首页 400-620-6333
400-620-6333
