This is a demo store. No orders will be fulfilled.
核酸电泳额外注意事项- 7大主题
在核酸电泳工作流程中,需要执行许多步骤,每一个步骤都可能影响核酸分离的结果,如前所述的实验设置部分所述。本页主题涉及与样品、试剂和运行参数相关的7个额外注意事项,包括:
1. 核酸序列和构象
2. 凝胶试剂性能
3. 凝胶厚度和孔的尺寸
4. 运行缓冲液类型
5. 凝胶运行时的电压、电流和功率
6. 核酸染色特性
7. 凝胶染色方法
一、核酸样品的序列和构象
电泳的基本原理表明,当核酸样品的大小不同时,它们具有不同的迁移率。然而,核苷酸数量相同但序列组成和构象不同的核酸在电泳过程中可能具有不同的迁移率(图1)。
富含AT的DNA可能比同样大小的富含GC的DNA迁移更慢,特别是在高分辨率电泳中。此外,大约每10 bp有4-6个腺苷重复的DNA分子(称为弯曲DNA)会不规则迁移,特别是在聚丙烯酰胺凝胶中[1,2]。它们的异常迁移可能是由于序列组成影响其分子构象。
构象:相同序列但不同构象的DNA分子的迁移,如圆形和线性化的质粒,受每个构象在通过凝胶孔时的紧致性的影响。高度紧凑的超卷曲分子迁移最快,其次是灵活的线性和开放的圆形分子(图1)。这种差异迁移可用于检测分离后质粒DNA的完整性,因为完整的质粒DNA在诸如转染哺乳动物细胞进行基因过表达等应用中是可取的。
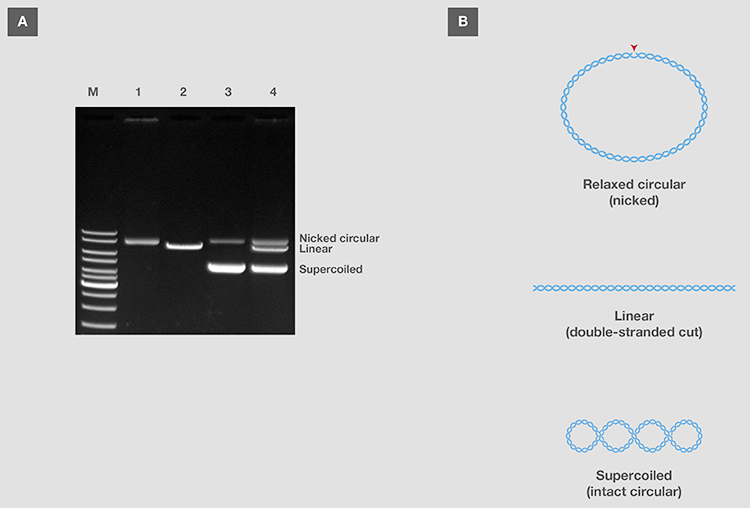
图1. 同一DNA在不同构象中的电泳迁移。(A)有缺口的圆形、线性和超卷曲质粒DNA的电泳。(B)松弛的圆形、线性和超卷曲质粒DNA的构象。被划破的质粒呈松弛、开放的圆形构象,体积最大,在凝胶中迁移最慢;线性化的质粒通过凝胶的速度略高;完整的超卷曲质粒最紧凑,迁移最快。
二、电泳需要考虑的琼脂糖和丙烯酰胺试剂的性质
要分离的核酸样本的大小和所需分辨率通常会驱动在琼脂糖凝胶或聚丙烯酰胺凝胶之间进行选择。一般来说,较高的凝胶比例对分解较小的分子更有效。表1总结了在选择用于核酸电泳的琼脂糖和丙烯酰胺凝胶试剂时需要考虑的性质。
表1. 与电泳相关的琼脂糖和丙烯酰胺凝胶试剂的性质[3,4]。
琼脂糖 | |
性能 | 影响 |
Clarity | 琼脂糖形成半透明的凝胶。 因此,在凝胶的 可视化和文档化 过程中,具有更高清晰度规格的琼脂糖可保证最小的荧光背景。 |
电渗透(EEO) | 电泳过程中,缓冲液离子与琼脂糖基质表面及里面电荷分子之间的相互作用,会影响缓冲液向电极的移动,这一过程被称为电渗或EEO。 由于缓冲液的正电离子(阳离子)与核酸(图2A)流动方向相反(图 2A),而带有较高负电荷的琼脂糖则会影响阳离子的移动,从而影响大核酸分子的分离(>10kb)。 |
凝胶点 | 凝胶点指的是琼脂糖溶液形成凝胶时的温度。 凝胶比例越高,凝胶点越高。 |
凝胶强度 | 凝胶强度用力单位(g/cm2)表示,指的是其抗破碎的能力,具体取决于琼脂糖浓度。 凝胶强度越高,就越方便处理。 |
遗传质量 | 遗传质量(GQ)指出,琼脂糖是否适用于分子生物学主要根据污染物和酶抑制剂水平。 |
熔点 | 熔点指的是琼脂糖的融化温度。 由于琼脂糖凝胶在受热时融化,所以熔点总是高于凝胶点。 低熔点琼脂糖(LMP) 是一种特殊琼脂糖,融化温度(~ 25°C)明显低于其他标准琼脂糖。 LMP琼脂糖同时具有较低的凝胶点,非常适用于大型核酸 提取和连接等胶内酶反应。 |
丙烯酰胺凝胶试剂 | |
性能 | 影响 |
分子生物学 | 使用已进行核酸酶活性和污染物存在测试的高质量,分子生物级试剂。可保护电泳过程中核酸样品的完整性。 |
稳定性/保质期 | 商业上通常在 聚丙烯酰胺原液中注入某种气体,以延长其稳定性。如果您在实验室自己制备聚丙烯酰胺原液,注意在几个月内使用完,否则其会随着时间推移分解为丙烯酸。 丙烯酰胺 和 双丙烯酰胺粉末或溶液应储存于避光容器中,以免受光线影响。 |
总的单体含量,w/v (%T) | 溶液中丙烯酰胺单体和交联双丙烯酰胺的总含量(% T)决定了聚丙烯酰胺凝胶的孔隙大小。 例如,10%的聚丙烯酰胺凝胶由10% (w/v) 的丙烯酰胺和双丙烯酰胺组成。 %T越高,孔隙越小,分离小分子的分辨率也就越高(了解更多: 聚丙烯酰胺凝胶推荐%)。 |
交联剂的百分比(%) | %C是指交联剂量与单体总量的比例(w/w)。 在指定%T中, %C越高,孔隙越小。 %C也指丙烯酰胺与双丙烯酰胺的比值(例如,5 %C为19:1)。 5% C(19:1)和3.3% C(29:1)的聚丙烯酰胺凝胶为核酸电泳常用凝胶。 |
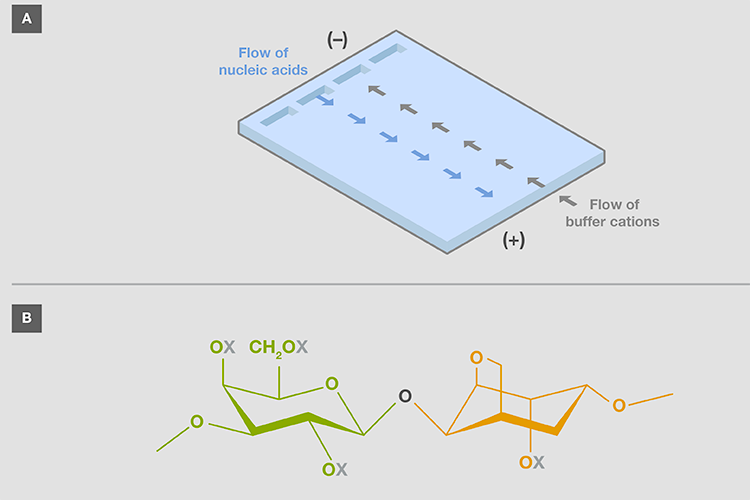
图2. (A)电泳过程中缓冲阳离子相对核酸的运动。(B)琼脂糖单元的结构,其在氧上的位置可能携带负电荷(用X表示)。
三、凝胶厚度和孔的尺寸
凝胶的厚度和孔的大小也可能影响电泳结果,琼脂糖和聚丙烯酰胺凝胶[3]。
一般来说,较厚的凝胶可能会导致带扩散,因为在凝胶运行过程中产生了更多的热量。由于凝胶染色背景高或染色和/或去除凝胶所需的时间长(如果进行了电泳后染色),也可能发生次优可视化。对于琼脂糖凝胶,厚度一般为3-4毫米,不建议超过5毫米的凝胶。聚丙烯酰胺凝胶的厚度由制造商提供的胶铸板垫片来确定,最常见的是0.75 mm, 1.0 mm和1.5 mm。
孔的大小,由凝胶梳的形状决定,不仅影响可以加载多少样品,而且影响条带的分辨率。虽然较大的孔可以容纳更多的样品负载,但它们可能会产生较厚的带,降低带分辨率并产生污点。另一方面,长而窄的孔可以容纳更小的样品量,但通常提供更清晰和更明确的波段,以获得更好的分辨率。更紧凑的样本也能从更少的输入中提供更高的频带强度。
四、运行缓冲类型
核酸电泳中常用的两种运行缓冲液是三乙酸EDTA (TAE)和三硼酸EDTA (TBE)[5]。低分子量样品(如DNA<1000 bp)用TBE缓冲液分离效果较好,具有较高的离子强度和缓冲能力;较大的DNA片段在TBE缓冲液中往往不能很好地分离。对于变性电泳,用于分解倾向于形成二级结构的分子,如RNA,通常使用TBE缓冲液;例如,聚丙烯酰胺凝胶主要由添加7-8 M尿素或类似变性剂的TBE缓冲液制备,以保持核酸的单链性。
对于较大分子量核酸(如DNA≥12-15 kb)的分离,首选TAE缓冲液和低场强(1-2 V/cm)。TAE缓冲液促进了凝胶的表观孔径增大,减少了电内渗作用(它是一种电荷相对较少的缓冲液),并降低了场强,所有这些都降低了大分子产生污点的趋势[6]。
五、电气运行参数:电压、电流、功率
用电泳分离样品时,施加电场使带负电的核酸向正极迁移。因此,控制电泳的电参数会影响样品的迁移及其组成片段的分辨率[7,8]。
从欧姆定律推导出的下列方程可用于表示电压(V)、电流(I)和功率(P)如何影响电泳结果。
电压=电流×电阻,或V = I × R
功率=电流x电压,或P = I x V
幂可以表示为P = I2 × R,因为V = I × R。
凝胶运行过程中的电阻(R)是系统固有的。例如,缓冲液(电导率和缓冲容量)、温度、凝胶性能(百分比、高度、长度、数量、截面)等,都影响系统的电阻。在导电介质中,当温度升高时,电阻降低,因为更高的温度允许更多的电流流动。然而,在凝胶运行过程中,阻力可能会发生变化。
电泳的另一个重要因素是热。产生的热量与系统消耗的功率成正比,并取决于缓冲电导率、施加电压和电阻。缓冲液的电导率越高(特别是由小离子组成时),电流流动越多。高电压和低电阻也增强了电流流动。总电流的上升增加了系统产生的功率和热量。
表2描述了电阻和热如何影响恒定电压、功率和电流对电泳系统的影响。无论电源设置的电气参数是什么,电压的上限应略低于系统可以处理的最大值,以避免过热和损坏设备和样品。一般的建议是设置足够高的电运行参数,以有效分离样品,而不会产生过多的热量。
表2. 电泳中的电压、功率和电流。
| 功率(P) | 电流(I) | |
描述 | V = I x R 对应凝胶系统两个电极间的电位差 | P = I x V or P = I2 x R 测量能量转换速率—其与系统产生的热量有关 | I = V/R 代表缓冲液离子的流动,与施加的电压直接相关 |
电泳的影响 | 电压影响电场强度(V/cm)。 高电压,可加快带电分子移动。 推荐使用恒压,以最大限度控制样品迁移速度。 既定系统中,电压恒定(V = I x R),电阻变化(例如,来自于不同数量和截面的凝胶)时电流相应减少或增加,以保持样品迁移速率相对恒定。 | 恒定功率可防止系统过热,但会导致样品迁移的不同。 在凝胶长时间的运行过程中,缓冲液离子(减少电流)的损耗可能导致电压逐渐增加,以保持恒定功率(P = I x V)。 蛋白质的等电聚焦(IEF) 是恒功率的典型应用。凝胶运行结束时,需逐渐增加电压,将样品“聚焦”到狭窄区域。 | 电流按2的数量级影响功率的大小(P = I2 x R)。 恒定电流可保持系统功耗和生成热量相对恒定(在核酸的连续非梯度凝胶中)。 在 非连续或梯度蛋白质凝胶电泳 中,恒定电流可能对样品堆积有用。 由于I = V/ R,当样品进入高百分比凝胶(电阻增加)时,为保持电流不变电压也应增加,此过程中对样品需施加更大的电场。 |
六、核酸荧光染料的一般性质
荧光染料常用于核酸样品电泳染色可视化。除了灵敏度外,染料的特性,如激发波长、结合亲和力和凝胶渗透速率,也会影响电泳的工作流程和应用(表3)[9]。
表3. 核酸染色用荧光染料的一般性质。
性能 | 影响 |
亲和力 | 染料的结合亲和力是一个重要的因素,因为染料与样品结合时经常观察到荧光增强。一般来说,核酸染料对双链分子(如DNA)的亲和力高于单链分子(如RNA),因为它更容易与双链螺旋结合。对于RNA电泳,对单链分子具有较高亲和力的独特染料可以提高RNA检测的特异性和敏感性。 |
变性剂的兼容性 | 尿素和甲酰胺是RNA电泳中典型的变性剂。在变性电泳中应考虑抗这些变性剂猝灭的染料,以提高效果。否则,变性凝胶在染色前应清洗以去除变性剂。 |
动态范围 | 动态范围表示发生线性检测样本量的数量级。因此,具有更大动态范围的染料可以更精确地定量凝胶中的条带。 |
激发波长 | 波长越长,能量越低,意味着对核酸的损伤越小。因此,蓝光激发的染料比紫外光激发的染料更能保护样品的完整性。这种影响可能会对下游应用程序产生显著影响,例如克隆效率。 |
凝胶渗透 | 当使用后电泳时,能更快穿透凝胶的染料不仅缩短了工作流程,还能更好地着色厚的和高百分比的凝胶。 |
内源荧光 | 具有低本征荧光的染料在凝胶染色中具有较低的背景,在改进检测的同时避免了需要去除的问题。 |
诱变 | 用于核酸染色的荧光染料由于具有插层特性,往往具有致突变性。那些已被证明诱变性较低并被归类为无害的染料应考虑增加安全性和方便处理。 |
七、染料与样品的结合:凝胶内和后电泳染色方法
两种常用的核酸样品染色方法是:
(1)凝胶内,将染色剂加入凝胶(和运行缓冲液)中
(2)电泳后,即凝胶在运行完成后在单独的浴池中染色
这两种方法各有优点和挑战,如表4所示。
表4. 凝胶内染色和电泳后染色的优点和考虑。
方法 | 优势 | 注意事项 |
凝胶内染色 | 更便利 工作流程更快 所需染色更少 | 在长时间运行后,染色可能会消失 染色剂只能使用一次 可能改变样品迁移性 |
电泳后染色 | 提供更精确的分子大小分析 允许重复使用染色液或多个凝胶同时染色 | 工作流程耗时长 所需染色剂较多 可能会产生较多有害废物 |
凝胶内染色更方便,需要的染料更少。然而,带正电荷的染色剂向与核酸相反的方向迁移,这可能会影响低分子量样品的检测,特别是在长时间的运行中(图3A)。此外,与核酸结合的染料可能会改变样品的迁移,这种现象被称为凝胶迁移,此时样品不符合大小(图3B)。此外,凝胶中含有的高水平插层染料可能改变超卷曲质粒DNA的构象,改变其在电泳中的迁移率(表观分子量)[10]。
由于电泳后染色在电泳过程中不影响样品,它是准确测定样品大小的首选方法。然而,这种方法增加了工作流程的时间,使用更多的染料,并在使用像溴化乙锭这样的染料时产生更多的有害废物。

图3. 插层染料核酸凝胶电泳结果。(A)凝胶中加入的溴化乙锭与核酸方向相反。黄线是荧光背景溴化乙锭与凝胶中染料耗尽的区域之间的边界。(B)当凝胶中加入大量插层染料时,与应用电泳后不同,会影响样品条带的迁移。为了说明这一效果,我们在两个凝胶中并排放置了两个梯子。高分子量阶梯(通道1)在两种凝胶中迁移相似(蓝线标记参考带,显示相似的条带位置)。电泳过程中,在染料存在的情况下,低分子量阶梯(2列)发生了不同的迁移。
总之,选择合适的试剂、参数和方法,以及工作流程设置,对于实现核酸分离和分析电泳的最佳结果至关重要。
参考文献
7.Thermo Fisher Scientific Inc. (2015) Protein Gel Electrophoresis Technical Handbook.
8.Sheehan D (2009) Electrophoresis. In: Physical Biochemistry: Principles and Applications. West Sussex: Wiley. pp 147–198.
9.Thermo Fisher Scientific Inc (2010) Nucleic Acid Detection and Analysis. In: Molecular Probes Handbook: A Guide to Fluorescent Probes and Labeling Technologies. pp 349–360.
 首页
首页 400-620-6333
400-620-6333
